Раньше голову, туловище, руки и посуду мыли мылом. Удобно. Один-два бруска мыла на всю семью и ок. Даже окна на зиму можно было на мыло заклеивать.
Сейчас зачем-то придумали шампунь, гель для душа, жидкое мыло для рук, средства для стирки отдельно, для мытья посуды отдельно.. Много всего, что дает пену и моет. Что во всех этих средствах общего?
Все они содержат ПАВ, поверхностно-активные вещества. ПАВ - этот тот самый компонент, который, собственно, моет и пенится. Это происходит за счёт того, что ПАВ дифильны, то есть, они одновременно гидрофильны и липофильны (гидрофобны и жирофобны, как хотите). Таким образом, можно считать, что ПАВ - это такие бисексуалы в мире веществ.
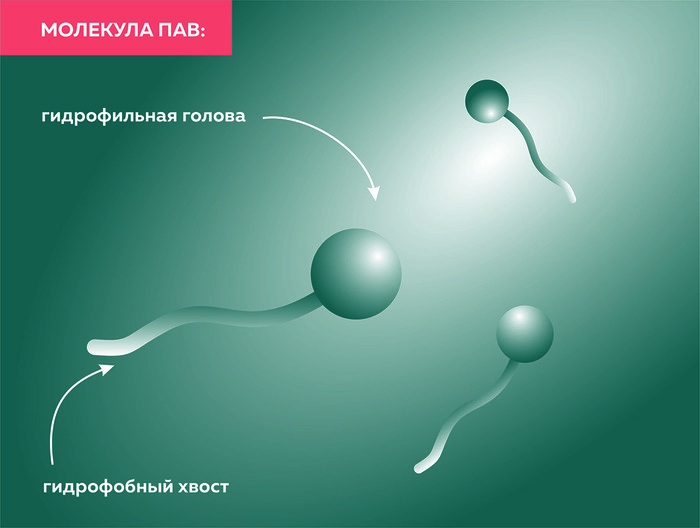
Такое неоднозначное отношение к воде обусловлено строением ПАВ. Все ПАВ имеют гидрофильную голову и гидрофобный хвост. И чо? А то, что загрязнения на коже, волосах, посуде, неважно, обычно являются жиром и в воде не растворяются.
Вот ПАВ своим жиролюбивым хвостом цепляют жирные загрязнения, заботливо окружают их, образуя мицеллу*, утаскивают в воду, а потом отправляют в путешествие по канализации.
*Оказавшись в воде, ПАВ образуют мицеллы, чтобы защитить гидрофобный хвост от контакта с водой. При этом мицеллы отталкиваются друг от друга, предотвращая слияние в мицеллищи.
Кроме того, ПАВ повышают смачиваемость поверхности, снижая поверхностное натяжение. Таким образом, вода лучше контактирует с загрязнениями. Кстати, строго говоря, эмульгатор - это тоже поверхностно-активное вещество.
Таким образом, главная функция шампуня - мыть волосы и кожу головы, удаляя кожное сало, пот, пыль и грязь. И только потом всё остальное, кондиционирование, придание объёма, разглаживание, избавление от перхоти, поход за пивом и тому подобные трюки.
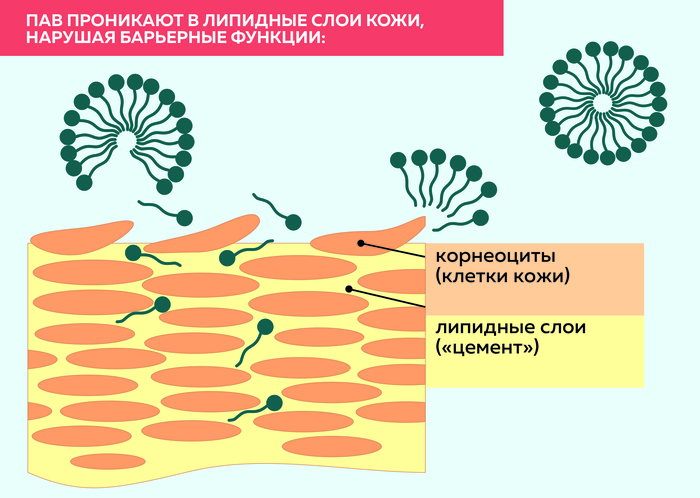
Однако, ПАВ довольно агрессивно удаляют не только грязь, но и собственные липиды кожи и волос, нарушая барьер. Наша кожа представляет собой отмершие клетки, склеенные жирами, кутикула волос устроена примерно по такому же принципу. Благодаря такой сложной организации, волосы прочные и блестящие, кожа гладкая и бархатистая. Вымывая липиды, ПАВ делают кожу более проницаемой, волосы тусклыми и ломкими, а настроение фиговым.
Предвосхищая вопрос о восстановлении. Видимый волос - мёртвый, он не имеет кровеносных сосудов и других штук, присущих живым частям тела. Живая часть волоска - луковица. Именно поэтому вернуть видимым волосам прочность и блеск после их повреждения силами организма невозможно:
Чем мельче мицелла и размер отдельных ПАВ, тем более агрессивным будет шампунь. Чтобы этого избежать, шампуни собирают из нескольких ПАВ. Кроме того, такой шампунь будет более густым и удобным в использовании и даст более пышную, приятную пену.
ТИПЫ ПАВ. Очень много текста
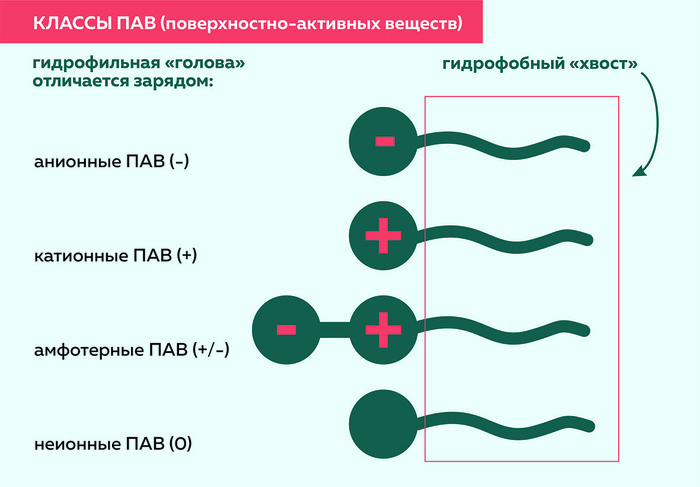
Поверхностно-активных веществ на сегодняшний день придумано огромное количество. И делят их на группы по заряду гидрофильной головы. Хвост этих молекул отличается не особо, обычно это какая-нибудь жирная кислота, полученная из масла кокоса или нефтепродуктов.
1) Анионные ПАВ - это соединения, которые, растворяясь в воде, образуют отрицательно (-) заряженные ионы, или анионы. Такие поверхностно-активные вещества отлично пенятся даже в жесткой воде. Как правило, анионный ПАВ – основное моющее вещество в шампуне, т.к. именно этот тип ПАВ лучше других справляется с загрязнениями.
Представители этого типа ПАВ обычно идут первыми в списке ингредиентов моющего средства, это, например, всем известные сульфатные ПАВ, такие как Sodium Lauryl Sulfate, Sodium Laureth Sulfate, Sodium Coco Sulfate и другие.
Сегодня многие не пользуются шампунями на основе сульфатных ПАВ (а зря), опасаясь их высокого раздражающего потенциала. На замену сульфатам пришли менее агрессивные изетионаты, сульфоацетаты и прочие *аты, например, Sodium Cocoyl Isethionate, Sodium Lauroyl Methyl Isethionate, Sodium Lauroyl Sarcosinate, Sodium Methyl Cocoyl Taurate и другие.
2) Катионные ПАВ, как правило, используются для создания кондиционеров и бальзамов для волос и заряжены положительно (+). Благодаря своему заряду, прекрасно кондиционируют и распутывают волосы, которые имеют анионный заряд. Обычно это какой-нибудь *тримониум или *димониум: Behentrimonium Methosulfate, Cetrimonium Chloride, Distearoylethyl Dimonium Chloride.
3) Неионные (неионогенные) ПАВ — это соединения, которые, растворяясь в воде, не образуют ионов. Имеют более слабую пенообразующую способность, чем анионники.
Но зато это очень щадящий тип поверхностно-активных веществ, считается, что некоторые из них можно даже не смывать. На флаконе их можно вычислить по названию: в шампуне часто можно увидеть глюкозиды: Lauryl Glucoside, Decyl Glucoside, Coco-Glucoside. Нередко попадаются и Cocamide DEA или Cocamide MEA.
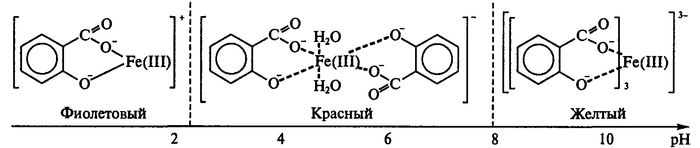
4) Амфотерные ПАВ. В зависимости от значения рН они проявляют свойства катионных (в кислой среде) или анионных (в щелочной среде) ПАВ. Обозначим их (+/-).
Они хорошо совместимы с анионными и катионными ПАВ, отлично пенятся, мягко воздействуют на кожу. Такие ПАВ применяются в шампунях «без слез», средствах для детей и людей с чувствительной кожей. Самый распространённые представители - Cocamidopropyl Betaine, Sodium Cocoamphoacetate. В сочетании с анионными ПАВ могут загущать систему (смесь) ПАВ, как правило, стоят на втором-третьем месте в списке ингредиентов.
Например, кокамидопропил бетаин (КАПБ) проявляет катионные свойства только в довольно кислой среде, при рН ближе к 3. При рН 5-6 КАПБ находится в своей цвиттер-ионной форме, то есть, количество положительно и отрицательно заряженных частиц в растворе одинаково и можно сказать, что при такой кислотности КАПБ имеет нейтральный заряд.
Итого, мы имеем: ПАВ бывают разные, в шампунях их совмещают для достижения идеального результата.
ПАВ могут агрессивно воздействовать на кожу головы и волосы, вымывая липиды. Негативное действие ПАВ сокращается, если пользоваться шампунями с мягкими ПАВ, смягчающими добавками (масла и поликватерниумы, особенно поликватерниум-10, сокращают вымывание липидов волос) или нанося перед мытьем на концы волос что-то, что защитит их, к примеру, масло или бальзам-ополаскиватель.
Думаю, пока хватит. Позже напишу, как составить рецепт шампуня и что там помимо ПАВ бывает. Всем спасибо, что дочитали)